ما الغاز الذي يعد مذيبًا للهواء الجوي

ما الغاز الذي يعد مذيبًا للهواء الجوي؟ وما هي خواصه؟ وما أهميته؟ ولماذا يعمل على إذابة الهواء؟ إن التعرُف على الغازات الموجودة في الهواء ليس كافيًا لنا، فهي تقوم بالعديد من التفاعلات التي قد لا نراها بالعين المُجردة، لذا تاليًا نضع لك النقاط على الحروف، ونُضيء لك هذا الطريق المجهول في التعرف على الهواء.
ما الغاز الذي يعد مذيبًا للهواء الجوي

الهواء الجوي ليس مُجرد هواء، بل يتكون من عدة غازات، هي الأكسجين بنسبة 21%، وثاني أكسيد الكربون بنسبة قليلة جدًا، أمّا العنصر الأعلى تركيز هو النيتروجين، لهذا يطلق عليه أنه الغاز الذي يعد مذيبًا للهواء الجوي، ومن خلال الجدول التالي سنتعرف على المعلومات الأساسية عن هذا الغاز:
| كثافته | الأعلى بين الغازات. |
| التركيز | 78% |
| الحالة | خامل |
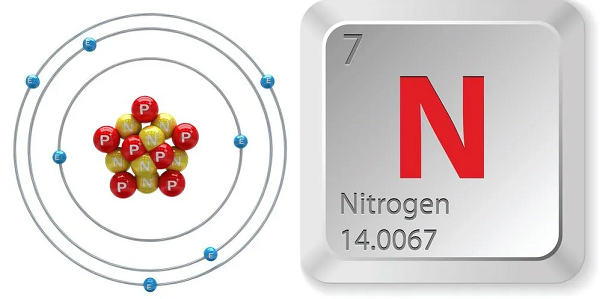
| الرمز | N |
| عدده الذري | 7 |
| المصفوفة | 15 |
لا يفوتك أيضًا: أي الغازات الآتية يسبب تكون المطر الحمضي
اكتشاف غاز النيتروجين
ظهر هذا العنصر باسمه لأول مرة في التاريخ على يد الطبيب والكيميائي “دانيال رذرفورد” بعام 1772، وكان هذا بسبب اكتشافُه لطريقة يزيل بها الأكسجين وثاني أكسيد الكربون من الهواء، وبهذا أصبح الغاز الذي يعد مذيبًا للهواء الجوي.
سمي بهذا الاسم نسبةً إلى الكلمة اللاتينية nitrum بدمجها مع الكلمة اليونانية Nitron، ولكن زادت على هذه التسمية اسم “الهواء المحترق” أو “الهواء النافث” التي أطلقت من قِبل العلماء “سكيل وكافنديش وبريستلي” اللذين تمكنوا من إعادة تجربة “راذرفورد” بذات العام.
الخواص الكيميائية لغاز النيتروجين
كونهُ الغاز الذي يعد مذيبًا للهواء الجوي ليس هو التفاعل الكيميائي الوحيد له، لذا فمن النقاط التالية يمكنك التعرف على الخواص الأخرى التي يقوم بها:
- النتروجين عديم اللون والرائحة.
- وزنه الذري 0067.
- كثافة النيتروجين هي N2 1.251 جرام / لتر، أمّا الكثافة النوعية 96737
- من العناصر التي يمكنها أن تكون سائلة وصلبة وغازية في آنٍ واحد، من خلال إيصال حرارته إلى -210.0 درجة مئوية أي ما يعادل 63 كلفن، ويكون بهذه الحالة بتركيز 12.6 كيلو باسكال.
- أمّا عند درجة الحرارة 77 كلفن يُمكن للنيتروجين السائل أن يتكثف في النيتروجين الغازي، مكونًا سائل يشبه الماء.
- النيتروجين له قدرة كهربية عالية جدًا تصل إلى 04، وهذا الرقم تم حسابُه على مقياس بولينج.
- درجة تجمد النيتروجين هي 63 كلفن، ويكون مادة تشبه الثلج المجروش ناعمًا.
- المدهش أن هذا المركب يوجد في الكثير من الأنظمة الحية.
- إذا لم يكن لديك نيتروجين سائل من الممكن تكوينه عن طريق الإسالة، والتقطير التجزيئي.
- يمكنك تكوينه من تسخين نتريت الأمونيوم.
- حالات الأكسدة التي تتكون من النيتروجين عددها تسعة.
- لدى النيتروجين القدرة على تشكيل روابط مع ذرات الفترة الثانية.
- لا يقدر النيتروجين على تشكيل مركبات كاتينية ثابتة.
- يتمكن النيتروجين من التفاعل مع العناصر الموجبة للكهرباء، مكونًا بهذا مواد صلبة.
- إذا ما تفاعلات الفلزات الكهربائية مع معه ينتج لنا نيتريد أيوني، وكلما قلت حساسية هذه المكونات للضوء يُصبح الناتج لدينا نيتريدًا بينيًا، وإذا قلت إلى أن أصبحت أشباه معادن ينتج منها نيتريد تساهمي.
- له القدرة على تكوين روابط ثلاثية مع أغلب المركبات، وهو العُنصر الذي ينتج منه أقوى الروابط الثلاثية على الإطلاق.
- ينتُج هذا العنصر من خلال المواد العضوية عقب تحللها، مكونًا بهذا نترات الصوديوم، ونترات البوتاسيوم، وهذه المركبات تكثر كلما كان المكان جافًا.
- أمّا الشكل غير العضوي منه يكون على هيئة (HNO3) وهي حمض النيتريك، أو (NH3 (وقد يظهر على هيئة الأكاسيد مثل (NO، NO2، N2O4، N2O) وفي أحيان قليلة أُخرى يكون على هيئة السيانيد CN-)).
وجود النيتروجين في الطبيعة
استكمالًا لإجابتنا على ما الغاز الذي يعد مذيبًا للهواء الجوي؟ يجدر بنا التطرق إلى الأماكن التي يوجد بها غير الهواء الجوي، فهو متغير ولا يوجد فقط في الهواء وإنما ينتشر في الطبيعة كلها كما يظهر في النقاط التالية:
- إذا تمت مقارنة العناصر الكيمائية بتواجدها في الطبيعة، نجد أن النيتروجين يحتل المرتبة السابعة في الانتشار.
- النيتروجين ليس متوفر بهذا القدر في القشرة الأرضية.
لا يفوتك أيضًا: عدد طبقات الغلاف الجوي
أهمية النيتروجين
عنصر بهذا القدر من التفاعلات والخواص، اهتم به العلماء كثيرًا للتعرف على الفائدة التي يمكنهم أن يحصدوها منه، وتوصلوا في النهاية إلى الفوائد الآتية:
أولًا: أهميته في للنبات
النيتروجين من العناصر التي تتواجد بكثرة في أوراق النباتات، وإذا ما فقدته فإن لونها يتحول إلى الأصفر في الحال، كما أن نموها يقف تمامًا، والثمار التي تنمو فيما بعد تكون صغيرة الحجم جدًا، لهذا السبب ظهرت لنا الأسمدة النيتروجينية.
بعد الكثير من الإحصاءات خرج لنا العلماء بنتيجة أن النسب الكبيرة منه في الزراعة قد تؤدي إلى تلويث المصارف الخاصة بالمياه، لكن المشكلة تكمن في أنه إذا توقفنا عن استخدام تلك الأسمدة فإننا بهذا نضحي بثلث المحصول الذي يخرج كل عام.
لهذا نبه العلماء على أن يكون استخدام أسمدة النيتروجين بشكل معتدل بحيث لا نفقد الفائدة ولا نحصد الضرر.
ثانيًا: أهميته للحياة
الكثيرين يعرفون فقط أن الغاز الذي يعد مذيبًا للهواء الجوي هو النيتروجين، وأن وظيفته تقتصر فقط على أنه أحد مكونات الهواء الذي نتنفسه، إلا أنها لا تنتهي وظيفته هنا.
- الأحماض النووية DNA وRNA النيتروجين يُعد عنصرًا أساسيًا فيهما، وبهذا يصبح النيتروجين مسيطرًا على أشكال الحياة المختلفة.
- يتم إضافته لبعض الأدوية كالمضادات الحيوية.
- يُعالج الثآليل الجلدية بسبب قدرته على التبريد.
- حفظ السائل المنوي والبويضات التي تستخدم في عمليات الحقن المجهري.
- من مركباته غاز أكسيد النيتروز N2O، الذي يسميه بعض الأطباء غاز الضحك، نسبةً إلى استخدامه كمخدر في العمليات الجراحية، وأكثر ما يتم استخدامه به هو طب الأسنان.
ثالثًا: الاستخدامات الصناعية
إن النيتروجين هو الغاز الذي يعد مذيبًا للهواء الجوي، وهذا الأمر يعني توافره بوفرة، ومن دون دفع الكثير، لهذا أصبح من العناصر التي ساعدت وبقوة على جعل الصناعة تسير إلى الأمام بسرعة كبيرة، ومن ضمن إسهاماته بها:
- في الصناعات الكيميائية كان يعمل كمبرد للتفاعلات الكيمائية، كما ساعد في نقلها، وكان يوقف بعض التفاعلات لفترة إن أراد المستخدمين ذلك.
- في إنتاج النفط، يتم إضافته إليه حتى يضغط عليه بقوة لكي يتم إنتاج أقصى ما يمكن استخراجه، كما يعد أفضل المكونات التي تقي من الانفجارات والحرائق الكبيرة.
- يستخدم في تلدين المعادن والمعالجة بالمواد الكيميائية الأخرى.
- في تصنيع الإلكترونيات من أجل منع التأكسد الذي يحدث أثناء تصنيع أشباه الموصلات أو الدوائر الكهربية.
- صناعة الزجاج تعتمد عليه بشكل كلي، حيث يبرد الإلكترود المتواجد بفرن تصنيع الزجاج، الأمر الذي يقي من حدوث التأكسد أثناء التصنيع.
رابعًا: استخدامات إضافية
لا يقتصر الأمر على الحياة التي يهبها لنا، وإنما الأمر يمكن أن يتطور ليصل إلى أننا قد نتخلى عن الكثير من الأمور بفقده، من تلك الاستخدامات التي ستفاجئك ما يلي:
- يستخدم النيتروجين في حث الأغذية على التجمد بسرعة كبيرة، وبتجميد الأدوية بهدف نقلها، وبالطبع في التجارب العضوية كافة.
- هو الغاز الذي يتم وضعه في الإطارات سواء للسيارات أو الإطارات، وتم اختياره هو بالذات لكونه لن يشتعل بعد الكثير من الاحتكاك.
- قد يوضع في المصابيح المتوهجة على سبيل التوفير، فغاز الآرغون باهظ الثمن جدًا.
- يستخدم بصناعة البارود.
أضرار النيتروجين
كما يحوي هذا الغاز الذي يعد مذيبًا للهواء الجوي العديد من الفوائد للبشرية، إلا أن له العديد من الأضرار التي لا يتوقعها أحد ولا يراها، والتي من بينها:
- الأكاسيد التي ينتجها النيتروجين في الهواء قبل الهطول ضارة جدًا، حيث تلوث الهواء وهي في طريقها للتربة.
- لا تنتج الأكاسيد فقط من الأمطار، وإنما من حرق الوقود كذلك، مثل الفحم والنفط.
- يُعتبر من الغازات التي تهيج الضباب الدخاني، ويحدث هذا بسبب أشعة الشمس التي تزيد من تفاعل أكاسيد النيتروجين مع الغلاف الجوي.
- المحركات النفاثة التي تطير في السماء تسبب وجود أكاسيد النيتروجين في الطبقات العليا بالغلاف، الأمر الذي يتلف الغلاف الجوي مع الوقت مسببًا الاحتباس الحراري وتتابع الكوارث الطبيعية التي تليه.
لا يفوتك أيضًا: ما الذي يغير الضغط الجوي
متى يكون النيتروجين سائلًا؟
تُعد هذه الحالة هي الأكثر استخدامًا للنيتروجين، حيث يصل لها بعد تبريده جدًا، عندها يكون خطرًا في التعامل معه، فهو سيكون قادر على تجميد أي شيء يلمسه، وإذا ما لُمس بالجلد يسبب تثليج الأنسجة، وهي حالة تضع الجزء الذي تم لمسه في موضع الخطر.
لهذا السبب تجد أغلب الباحثين في حين التعامل معه يرتدون قفازات في سبيل حماية أيديهم، وقد تم اكتشاف هذه القدرة على التجمد في القرن التاسع عشر، من وقتها وأكثر ما اشتُهر به استخدامُه في الغذاء، فتم الاستعانة به في صناعة الآيس كريم ذاك النوع الذي نراه بالصور يتصاعد منه الدخان.
كما يوضع على بعض الحلويات بنسب معينة كي تعطي لها مظهرًا شهيًا، وانتشرت هذه الاستخدامات المباشرة له رغم الخطورة الكبيرة، لهذا خرجت منظمة الغذاء والدواء الأمريكية في ببيان واضح أن استخدامه بهذا الشكل الصريح خطرٌ على صحة الإنسان ويؤثر على الأجزاء الداخلية للجسم، حتى لو تم وضعه بنسب صغيرة.
